Для характеристики окислительно-восстановительной способности частиц важное значение имеет такое понятие, как степень окисления. СТЕПЕНЬ ОКИСЛЕНИЯ – это заряд, который мог бы возникнуть у атома в молекуле или ионе, если бы все его связи с другими атомами оказались разорваны, а общие электронные пары ушли с более электроотрицательными элементами.
В отличие от
реально существующих зарядов у ионов,
степень окисления показывает лишь
условный заряд атома в молекуле. Она
может быть отрицательной, положительной
и нулевой. Например, степень окисления
атомов в простых веществах равна «0»
(, ,
, ,
, ).
В химических соединениях атомы могут
иметь постоянную степень окисления или
переменную. У металлов главных подгруппI,
II
и III
групп Периодической системы в химических
соединениях степень окисления, как
правило, постоянна и равна соответственно
Ме +1 ,
Ме +2
и Ме +3
(Li + ,
Ca +2 ,
Al +3).
У атома фтора всегда -1. У хлора в
соединениях с металлами всегда -1. В
подавляющем числе соединений кислород
имеет степень окисления -2 (кроме
пероксидов, где его степень окисления
-1), а водород +1(кроме гидридов металлов,
где его степень окисления -1).
).
В химических соединениях атомы могут
иметь постоянную степень окисления или
переменную. У металлов главных подгруппI,
II
и III
групп Периодической системы в химических
соединениях степень окисления, как
правило, постоянна и равна соответственно
Ме +1 ,
Ме +2
и Ме +3
(Li + ,
Ca +2 ,
Al +3).
У атома фтора всегда -1. У хлора в
соединениях с металлами всегда -1. В
подавляющем числе соединений кислород
имеет степень окисления -2 (кроме
пероксидов, где его степень окисления
-1), а водород +1(кроме гидридов металлов,
где его степень окисления -1).
Алгебраическая сумма степеней окисления всех атомов в нейтральной молекуле равна нулю, а в ионе – заряду иона. Эта взаимосвязь позволяет рассчитывать степени окисления атомов в сложных соединениях.
В молекуле серной
кислоты H 2 SO 4
атом водорода имеет степень окисления
+1, а атом кислорода -2. Так как атомов
водорода два, а атомов кислорода четыре,
то мы имеем два «+» и восемь «-». До
нейтральности не хватает шесть «+».
Именно это число и является степенью
окисления серы -
 .
Молекула дихромата калияK 2 Cr 2 O 7
состоит из двух атомов калия, двух атомов
хрома и семи атомов кислорода. У калия
степень окисления всегда +1, у кислорода
-2. Значит, мы имеем два «+» и четырнадцать
«-». Оставшиеся двенадцать «+» приходятся
на два атома хрома, у каждого из которых
степень окисления равна +6 (
.
Молекула дихромата калияK 2 Cr 2 O 7
состоит из двух атомов калия, двух атомов
хрома и семи атомов кислорода. У калия
степень окисления всегда +1, у кислорода
-2. Значит, мы имеем два «+» и четырнадцать
«-». Оставшиеся двенадцать «+» приходятся
на два атома хрома, у каждого из которых
степень окисления равна +6 ( ).
).
Типичные окислители и восстановители
Из определения процессов восстановления и окисления следует, что, в принципе, в роли окислителей могут выступать простые и сложные вещества, содержащие атомы, которые находятся не в низшей степени окисления и поэтому могут понижать свою степень окисления. Аналогично в роли восстановителей могут выступать простые и сложные вещества, содержащие атомы, которые находятся не в высшей степени окисления и поэтому могут повышать свою степень окисления.
К наиболее сильным окислителям относятся:
1) простые вещества, образуемые атомами, имеющими большую электроотрицательность, т.е. типичные неметаллы, расположенные в главных подгруппах шестой и седьмой групп периодической системы: F, O, Cl, S (соответственно F 2 , O 2 , Cl 2 , S);
2) вещества, содержащие элементы в высших и промежуточных
положительных степенях окисления, в том числе в виде ионов, как простых, элементарных (Fe 3+), так и кислородосодержащих, оксоанионов (перманганат-ион - MnO 4 -);
3) перекисные соединения.
Конкретными
веществами, применяемыми на практике
в качестве окислителей, являются кислород
и озон, хлор, бром, перманганаты, дихроматы,
кислородные кислоты хлора и их соли
(например,
 ,
, ,
, ),
азотная кислота (
),
азотная кислота ( ),
концентрированная серная кислота
(
),
концентрированная серная кислота
( ),
диоксид марганца (
),
диоксид марганца ( ),
пероксид водорода и пероксиды металлов
(
),
пероксид водорода и пероксиды металлов
(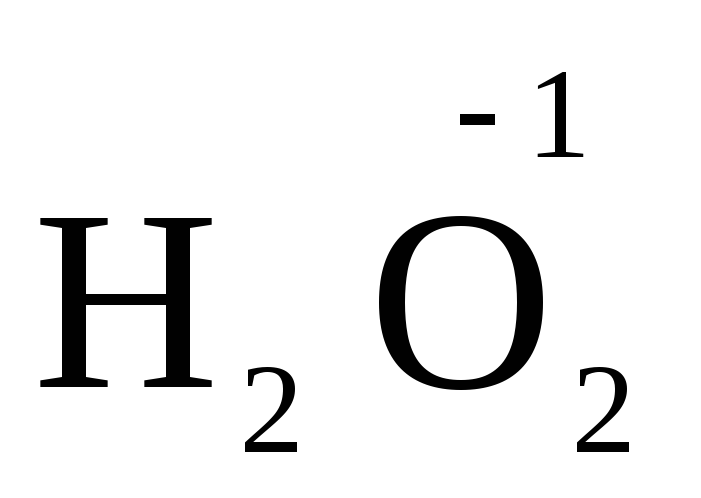 ,
, ).
).
К наиболее сильным восстановителям относятся:
1)простые вещества, атомы которых имеют низкую электроотрицательность («активные металлы»);
2) катионы металлов в низжих степенях окисления (Fe 2+);
3) простые элементарные анионы, например, сульфид-ион S 2- ;
4) кислородосодержащие
анионы (оксоанионы), соответствующие
низшим положительным степеням окисления
элемента (нитрит
 ,
сульфит
,
сульфит ).
).
Конкретными
веществами, применяемыми на практике
в качестве восстановителей, являются,
например, щелочные и щелочноземельные
металлы, сульфиды, сульфиты, галогенводороды
(кроме HF),
органические вещества – спирты,
альдегиды, формальдегид, глюкоза,
щавелевая кислота, а также водород,
углерод, моноксид углерода ( )
и алюминий при высоких температурах.
)
и алюминий при высоких температурах.
В принципе, если в состав вещества входит элемент в промежуточной степени окисления, то эти вещества могут проявлять как окислительные, так и восстановительные свойства. Все зависит от
«партнера» по реакции: с достаточно сильным окислителем оно может реагировать как восстановитель, а с достаточно сильным восстановителем – как окислитель. Так, например, нитрит-ион NO 2 - в кислой среде выступает в роли окислителя по отношению к иону I - :
2 +
2
+
2 + 4HCl→
+ 4HCl→
 +
2
+
2 + 4KCl
+ 2H 2 O
+ 4KCl
+ 2H 2 O
и в роли восстановителя по отношению к перманганат-иону MnO 4 -
5 +
2
+
2 + 3H 2 SO 4
→ 2
+ 3H 2 SO 4
→ 2 +
5
+
5 +K 2 SO 4
+ 3H 2 O
+K 2 SO 4
+ 3H 2 O
Цель: Продолжить изучение валентности. Дать понятие степени окисления. Рассмотреть виды степеней окисления: положительная, отрицательная, нулевой значение. Научиться правильно, определять степени окисления атома в соединении. Научить приемам сравнения и обобщения изучаемых понятий; отработать умения и навыки в определении степени окисления по химическим формулам; продолжить развитие навыков самостоятельной работы; способствовать развитию логического мышления. Формировать чувство толерантности (терпимости и уважения к чужому мнению) взаимопомощи; осуществлять эстетическое воспитание (через оформление доски и тетрадей, при применении презентаций).
Ход урока
I . Организационный момент
Проверка учащихся к уроку.
II . Подготовка к уроку.
К уроку понадобятся: Периодическая система Д.И.Менделеева, учебник, рабочие тетради, ручки, карандаши.
III . Проверка домашнего задания .
Фронтальный опрос, некоторые будут работать у доски по карточкам, проведение теста, и подведением данного этапа будет интеллектуальная игра.
1. Работа с карточками.
1 карточка
Определить массовые доли (%) углерода и кислорода в углекислом газе (СО 2 ) .
2 карточка
Определить тип связи в молекуле Н 2 S. Написать структурную и электронную формулы молекулы.
2. Фронтальный опрос
- Что называется химической связью?
- Какие виды химических связей вы знаете?
- Какая связь называется ковалентной связью?
- Какие ковалентные связи выделяют?
- Что такое валентность?
- Как мы определяем валентность?
- Какие элементы (металлы и неметаллы) имеют изменчивую валентность?
3. Тестирование
1. В каких молекулах существует неполярная ковалентная связь?
2 . У какой молекулы при образовании ковалентно-неполярной связи образуется тройная связь?
3 . Как называется положительно заряженные ионы?
А) катионы
Б) молекулы
В) анионы
Г) кристаллы
4. В каком ряду располагаются вещества ионного соединения?
А) СН 4 , NН 3 , Мg
Б) СI 2 , МgО, NаСI
В) МgF 2 , NаСI, СаСI 2
Г) Н 2 S, НСI, Н 2 О
5 . Валентность определяются по:
А) по номеру группы
Б) по числу неспаренных электронов
В) по типу химической связи
Г) по номеру периода.
4. Интеллектуальная игра «Крестики-нолики »
Найдите вещества с ковалентно-полярной связь.
IV . Изучение нового материала
Степень окисления является важной характеристикой состояния атома в молекуле. Валентность, определяется по числу неспаренных электронов в атоме, орбиталями с неподеленными электронными парами, только в процессе возбуждения атома. Высшая валентность элемента, как правило, равна номеру группы. Степень окисления в соединениях с разными химическими связями образуется неодинаково.
Как образуется степень окисления у молекул с разными химическими связями?
1) В соединениях с ионной связью степени окисления элементов равно зарядам ионов.
2) В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степень окисления элементов равно 0.
Н 2 0 , С I 2 0 , F 2 0 , S 0 , AI 0
3) У молекул с ковалентно-полярной связью степень окисления определяется подобно молекулам с ионной химической связью.
Степень окисления элемента – это условный заряд его атома, в молекуле, если считать, что молекула состоит из ионов.
Степень окисления атома в отличие от валентности имеет знак. Она может быть положительной, отрицательной и нулевой.
Валентность обозначатся римскими цифрами сверху символа элемента:
II |
I |
IV |
Fe |
Cu |
S , |
а степень окисления обозначается арабскими цифрами с зарядом над символам элемента (М g +2 , Са +2 , N а +1 , CI ˉ¹).
Положительная степень окисления – равна числу электронов, отданных данным атомам. Атом может отдать все валентные электроны (для главных групп это электроны внешнего уровня) соответствующее номеру группы, в котором находится элемент, проявляя при этом высшую степень окисления (исключение ОF 2).Например: высшая степень окисления главной подгруппы II группы равна +2 (Zn +2) Положительную степень проявляют как металлы и неметаллы, кроме F, He, Ne.Например: С+4 , Na +1 , Al +3
Отрицательная степень окисления равна числу электронов, принятых данным атомом, ее проявляют только неметаллы. Атомы неметаллов присоединяют столько электронов, сколько их не хватает до завершения внешнего уровня, проявляя при этом отрицательную степень.
У элементов главных подгрупп IV-VII групп минимальная степень окисления численно равна
Например:
Значение степени окисления между высшим и низшим степенями окислений называется промежуточными:
Высшая |
Промежуточные |
Низшая |
С +3 , С +2 ,С 0 ,С -2 |
||
В соединениях с ковалентной неполярной связью (в молекулах простых веществ) степень окисления элементов равно 0: Н 2 0 , С I 2 0 , F 2 0 , S 0 , AI 0
Для определения степени окисления атома в соединении следует учитывать ряд положений:
1. Степень окисления F во всех соединениях равна « -1». Na +1 F -1 , H +1 F -1
2. Степень окисления кислорода в большинстве соединений равна (-2) исключение: О F 2 , где степень окисления О +2 F -1
3. Водород в большинстве соединений имеет степень окисления +1, кроме соединения с активными металлами, где степень окисления (-1) : Na +1 H -1
4.Степень окисления металлов главных подгрупп I , II , III групп во всех соединениях равна +1,+2,+3.
Элементы с постоянной степенью окисления это:
А) щелочные металлы (Li, Na, K, Pb, Si, Fr) - степень окисления +1
Б) элементы II главной подгруппы группы кроме (Hg): Be, Mg, Ca, Sr, Ra, Zn, Cd - степень окисления +2
В) элемент III группы: Al - степень окисления +3
Алгоритм составления формулы в соединениях:
1 способ
1 . На первом месте пишется элемент с меньшей электроотрицательностью, на втором с большей электроотрицательностью.
2 . Элемент, написанный на первом месте имеет положительный заряд «+», а на втором с отрицательным зарядом «-».
3 . Указать для каждого элемента степень окисления.
4 . Найти общее кратное значение степеней окисления.
5. Разделить наименьшее общее кратное на значение степеней окисления и полученные индексы приписать внизу справа после символа соответствующего элемента.

6. Если степень окисления четное – нечетное, то они становятся рядом с символом справа внизу крест – накрест без знака «+» и «-»:
![]()
7. Если степень окисления имеет четное значение, то их сначала нужно сократить на наименьшее значение степени окисления и поставить крест – накрест без знака «+» и «-»: С +4 О -2

2 способ
1 . Обозначим степень окисления N через Х, указать степень окисления О: N 2 x O 3 -2
2 . Определить сумму отрицательных зарядов, для этого степень окисления кислорода умножаем на индекс кислорода: 3· (-2)= -6
3 .Чтобы молекула была электронейтральной нужно определить сумму положительных зарядов: Х2 = 2Х
4 .Составить алгебраическое уравнение:
N 2 + 3 O 3 –2
V . Закрепление
1) Проведение закрепления темы игрой, которое называется «Змейка».
Правила игры: учитель раздает карточки. На каждой карточке написан один вопрос и один ответ на другой вопрос.
Учитель начинает игру. Зачитает вопрос, ученик, у которого на карточке есть, ответ на мой вопрос поднимает руку и говорит ответ. Если ответ правильный, то он читает свой вопрос и у того ученика у которого есть ответ на этот вопрос поднимает руку и отвечает и т.д. Образуется змейка правильных ответов.
- Как и где обозначается степень окисления у атома химического элемента?
Ответ : арабской цифрой над символом элемента с зарядом «+» и «-». - Какие виды степеней окисления выделяют у атомов химических элементов?
Ответ : промежуточная - Какую степень проявляет металлы?
Ответ : положительная, отрицательная, нулевая. - Какую степень проявляют простые вещества или молекулы с неполярной ковалентной связью.
Ответ : положительная - Какой заряд имеют катионы и анионы?
Ответ : нулевое. - Как называется степень окисления, которая стоит между положительным и отрицательным степенями окисления.
Ответ : положительный,отрицательный
2) Написать формулы веществ состоящих из следующих элементов
- N и H
- Р и О
- Zn и Cl
3) Найти и зачеркнуть вещества, не имеющие переменчивую степень окисления.
Na, Cr, Fe, K, N, Hg, S, Al, C
VI . Итог урока.
Выставление оценок с комментариями
VII . Домашнее задание
§23, стр.67-72, задание после §23-стр 72 №1-4 выполнить.
Таблица. Степени окисления химических элементов.
Таблица. Степени окисления химических элементов.
Степень окисления
- это условный заряд атомов химического элемента в соединении, вычисленный из предположения, что все связи имеют ионный тип. Степени окисления могут иметь положительное, отрицательное или нулевое значение, поэтому алгебраическая сумма степеней окисления элементов в молекуле с учётом числа их атомов равна 0, а в ионе - заряду иона
.
|
Таблица: Элементы с неизменными степенями окисления. |
|
Таблица. Степени окисления химических элементов по алфавиту.
|
Таблица. Степени окисления химических элементов по номеру.
|
Оценка статьи:
Как определить степень окисления? Таблица Менделеева позволяет записывать данную количественную величину для любого химического элемента.
Определение
Для начала попробуем понять, что представляет собой данный термин. Степень окисления по таблице Менделеева представляет собой количество электронов, которые приняты либо отданы элементом в процессе химического взаимодействия. Она может принимать отрицательное и положительное значение.
Связь с таблицей
Как определяется степень окисления? Таблица Менделеева состоит из восьми групп, расположенных вертикально. В каждой из них есть две подгруппы: главная и побочная. Для того чтобы установить показатели для элементов, необходимо использовать определенные правила.

Инструкция
Как рассчитать степени окисления элементов? Таблица позволяет в полной мере справиться с подобной проблемой. Щелочные металлы, которые располагаются в первой группе (главной подгруппе), степень окисления проявляют в соединениях, она соответствует +, равна их высшей валентности. У металлов второй группы (подгруппы А) +2 степень окисления.
Таблица позволяет определить данную величину не только у элементов, проявляющих металлические свойства, но и у неметаллов. Их максимальная величина будет соответствовать высшей валентности. Например, для серы она составит +6, для азота +5. Как вычисляется у них минимальная (низшая) цифра? Таблица отвечает и на этот вопрос. Необходимо вычесть номер группы из восьми. Например, у кислорода она составит -2, у азота -3.
Для простых веществ, которые не вступали в химическое взаимодействие с другими веществами, определяемый показатель считается равным нулю.
Попробуем выявить основные действия, касающиеся расстановки в бинарных соединениях. Как поставить в них степень окисления? Таблица Менделеева помогает решить проблему.
Для примера возьмем оксид кальция СаО. Для кальция, расположенного в главной подгруппе второй группы, величина будет являться постоянной, равной +2. У кислорода, имеющего неметаллические свойства, данный показатель будет являться отрицательной величиной, и он соответствует -2. Для того чтобы проверить правильность определения, суммируем полученные цифры. В итоге мы получим ноль, следовательно, вычисления верны.
Определим подобные показатели еще в одном бинарном соединении CuO. Так как медь располагается в побочной подгруппе (первой группе), следовательно, изучаемый показатель может проявлять разные значения. Поэтому для его определения необходимо сначала выявить показатель для кислорода.
У неметалла, располагающегося в конце бинарной формулы, степень окисления имеет отрицательное значение. Так как этот элемент располагается в шестой группе, при вычитании из восьми шести получаем, что степень окисления у кислорода соответствует -2. Так как в соединении отсутствуют индексы, следовательно, показатель степени окисления у меди будет положительным, равным +2.
Как еще используется химическая таблица? Степени окисления элементов в формулах, состоящих из трех элементов, также вычисляются по определенному алгоритму. Сначала расставляют эти показатели у первого и последнего элемента. Для первого этот показатель будет иметь положительное значение, соответствовать валентности. У крайнего элемента, в качестве которого выступает неметалл, данный показатель имеет отрицательное значение, он определяется в виде разности (от восьми отнимают номер группы). При вычислении степени окисления у центрального элемента используют математическое уравнение. При расчетах учитывают индексы, имеющиеся у каждого элемента. Сумма всех степеней окисления должна быть равна нулю.

Пример определения в серной кислоте
Формула данного соединения имеет вид H 2 SO 4 . У водорода степень окисления составит +1, у кислорода она равна -2. Для определения степени окисления у серы, составим математическое уравнение: + 1 * 2 + Х + 4 * (-2) = 0. Получаем, что степень окисления у серы соответствует +6.

Заключение
При использовании правил можно расставлять коэффициенты в окислительно-восстановительных реакциях. Данный вопрос рассматривается в курсе химии девятого класса школьной программы. Кроме того, информация о степенях окисления позволяет выполнять задания ОГЭ и ЕГЭ.
Видеокурс «Получи пятерку» включает все темы, необходимые для успешной сдачи ЕГЭ по математике на 60-65 баллов. Полностью все задачи 1-13 Профильного ЕГЭ по математике. Подходит также для сдачи Базового ЕГЭ по математике. Если вы хотите сдать ЕГЭ на 90-100 баллов, вам надо решать часть 1 за 30 минут и без ошибок!
Курс подготовки к ЕГЭ для 10-11 класса, а также для преподавателей. Все необходимое, чтобы решить часть 1 ЕГЭ по математике (первые 12 задач) и задачу 13 (тригонометрия). А это более 70 баллов на ЕГЭ, и без них не обойтись ни стобалльнику, ни гуманитарию.
Вся необходимая теория. Быстрые способы решения, ловушки и секреты ЕГЭ. Разобраны все актуальные задания части 1 из Банка заданий ФИПИ. Курс полностью соответствует требованиям ЕГЭ-2018.
Курс содержит 5 больших тем, по 2,5 часа каждая. Каждая тема дается с нуля, просто и понятно.
Сотни заданий ЕГЭ. Текстовые задачи и теория вероятностей. Простые и легко запоминаемые алгоритмы решения задач. Геометрия. Теория, справочный материал, разбор всех типов заданий ЕГЭ. Стереометрия. Хитрые приемы решения, полезные шпаргалки, развитие пространственного воображения. Тригонометрия с нуля - до задачи 13. Понимание вместо зубрежки. Наглядное объяснение сложных понятий. Алгебра. Корни, степени и логарифмы, функция и производная. База для решения сложных задач 2 части ЕГЭ.

